Co je to elektrolýza vody?
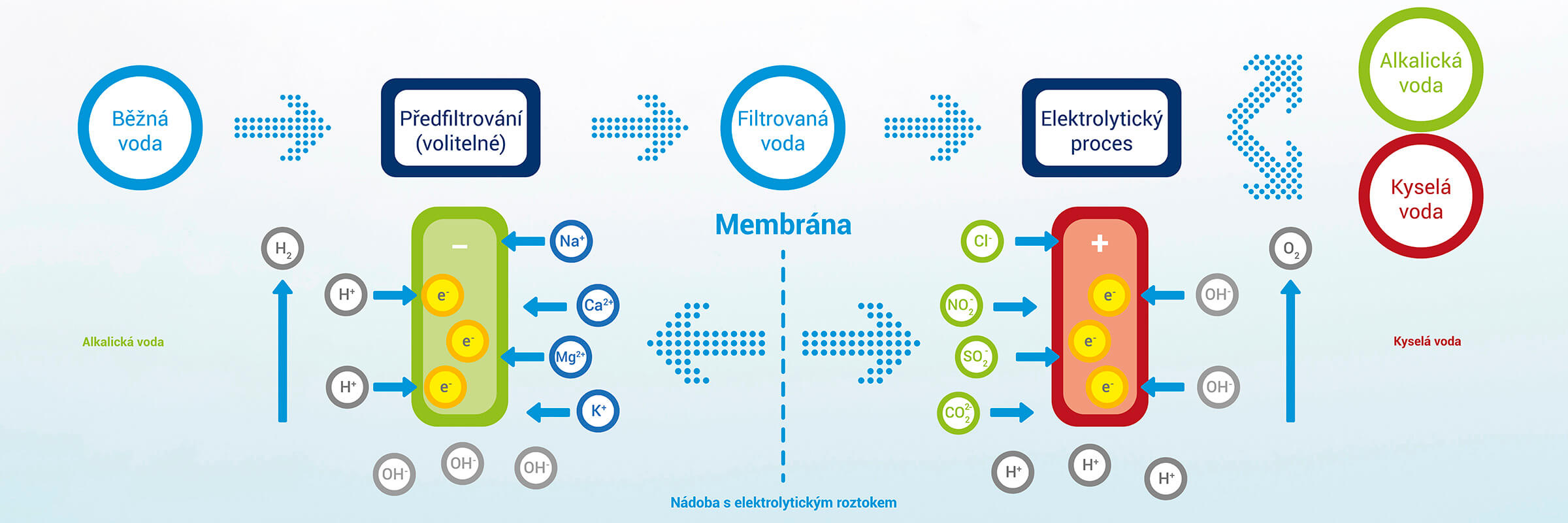
Co to je elektrolýza
Elektrolýza je děj, při kterém dochází k rozkladu roztoku elektrolytu (tavenina nebo roztok iontových sloučenin) procházejícím stejnosměrným elektrickým proudem. Proud je do roztoku zaváděn pomocí dvojice elektrod – katody a anody. Proud způsobuje, že na elektrodách dochází k oxidačně-redukčním (redoxním) reakcím.
ArchivPodobné
Jak funguje Elektrolyza
Principem elektrolýzy je rozklad vody na vodík a kyslík pomocí elektrické energie. Opakem této technologie je palivový článek (PČ), kde dochází k přímé přeměně energie chemické na energii elektrickou. Palivové články produkují minimální množství emisí ve srovnání se stávajícími technologiemi využívání fosilních paliv.
Archiv
Na čem probíhá elektrolýza
Elektrolýza je děj, který probíhá na elektrodách při průchodu stejnosměrného elektrického proudu roztokem nebo taveninou. Aby tento děj mohl probíhat, musí být v roztoku nebo tavenině obsaženy volně pohyblivé ionty. Ke kladné elektrodě, anodě (+) směřují svůj pohyb záporně nabité ionty, anionty.
Archiv
Co se stane když se iont dotkne elektrody
Záporně nabité ionty se pohybují ke kladné elektrodě (anodě) a proto se nazývají anionty. Když anionty a kationty dosáhnou elektrod, předají jim své náboje (anionty odevzdají elektrony, kationty je naopak získají) a tak se stanou neutrálními atomy či molekulami.
Jak vzniká elektrolyt
Elektrolyty jsou roztoky nebo taveniny, které vedou elektrický proud. Vznikají obvykle rozpuštěním iontových sloučenin v polárních rozpouštědlech. V elektrolytech nepřenášejí proud elektrony jako u kovů (vodičů I. řádu), ale ionty.
Jak se počítá elektrolýza
Elektrochemický ekvivalent určíme podle vzorce: A= M m F⋅ .
Co se vylučuje při elektrolýze
Při elektrolýze se uvolňují bublinky, vznikají dva plyny, chlor Cl2 na kladné elektrodě, vodík H2 na záporné elektrodě. Tím se z roztoku odstraňují chloridové anionty Cl- a kationty vodíku H+. V misce vzniká z iontů H+ a OH- hydroxid sodný NaOH.
Jak oddělit vodík od vody
Elektrolýza je v současné době považována za nejslibnější metodu výroby vodíku rozkladem vody, a to zejména díky vysoké efektivitě konverze, intenzitě a technologické jednoduchosti procesu v porovnání s alternativními způsoby (termochemickými procesy či fotokatalýzou).
Jak si vyrobit elektrolýzu
Do plastové nádoby nalijeme vodu a v poloměru15 až 20ti % nasipeme sůl da se to trefit i od oka. Na trafo připojíme kabely které jsou připojeny na plus a mínus . Na plus pól připojíme měděnou tyč nebo drát a ponořime tyč či drát do vody tak aby krokodýlek byl nad hladinou.
Kde se v praxi používá elektrolýza
Využití elektrolýzy
polarografie – určování chemického složení látky pomocí změn elektrického proudu procházejícího roztokem zkoumané látky; akumulátory – nabíjení chemického zdroje elektrického napětí průchodem elektrického proudu.
Kde se nachází elektrolyt
Elektrolyty jsou ionizované minerály, které se nachází v krvi, moči a potu. Jde o látky, které po rozpuštění ve vodě získávají kladný či záporný náboj. Umožňují přenos vzruchu v krvi, vnitrobuněčných i mezibuněčných tekutinách a zásadním způsobem ovlivňují většinu metabolických procesů v organismu.
Co obsahuje elektrolyt
Zdroje elektrolytůkokosová voda (draslík, sodík)jahody, meruňky, dřín obecný, borůvky, brusinky, arónie, moruše.granátové jablko, granátová šťáva (hořčík, draslík, sodík a vápník)ananas (draslík, hořčík, vápník)mandle.chřest, česnek, celer.avokádo.dýně, konopná semínka, lněná semínka.
Kdy byla vynalezena elektrolýza
S baterií o 2000 článcích se mu podařilo objevit roku 1811 uhlíkový elektrický oblouk (1811), který pak sloužil jako elektrický zdroj světla až do roku 1879, kdy T. A. Edison sestrojil žárovku. M. Faraday roku 1834 objevil dva základní zákony elektrolýzy, které nesou jeho jméno.
Proč má vodík vznikající při elektrolýze vody větší objem než kyslík
Na katodě (záporná elektroda) vzniká vodík, na anodě (kladná elektroda) se vylučuje kyslík. Objemy plynů jsou v poměru 2:1. Určité množství vzniklého kyslíku se rozpouští ve vodě, tudíž objem vzniklého vodíku se může jevit více než dvojnásobný.
Jak funguje vodíková elektrárna
Vodíková mobilita dnes funguje na principu palivových článků, které vyrábí elektřinu přímou elektrochemickou reakcí vodíku a kyslíku na vodu. Jako odpadní látka tak vzniká pouze demineralizovaná voda a vzduch, který je pročištěn filtry. S trochou nadsázky tak lze říct, že vodíkové automobily čistí planetu.
Kde se nachází vodík
Vodík je základním stavebním prvkem celého vesmíru, vyskytuje se jak ve všech svítících hvězdách, tak v mezigalaktickém prostoru. Podle současných měření se podílí ze 75 % na hmotě a dokonce z 90 % na počtu atomů přítomných ve vesmíru.
Jak získat elektrolyty
Jednou z nejjednodušších a nejúčinnějších metod, jak získat elektrolyty, je zdravý a vyvážený jídelníček, který obsahuje hromadu na elektrolyty bohatých potravin, jako je ovoce, zelenina, luštěniny, tučnější ryby, avokádo, oříšky nebo semínka.
Jak poznat silný elektrolyt
Elektrolyty silné
jsou takové elektrolyty ve kterých prakticky dochází k rozštěpení všech chemických vazeb v původních látkách a ke vzniku volně pohyblivých iontů. U silných elektrolytů prakticky neexistují nedisociované molekuly původně rozpouštěné látky.
Jak získat vodík z vody
Při elektrolýze vody se průchodem elektrického proudu roztokem štěpí vazby mezi vodíkem a kyslíkem a voda se tak rozkládá na tyto dva plyny. Celková účinnost tohoto procesu se pohybuje okolo 55–60 %. Na výrobu 1 kg vodíku elektrolýzou je zapotřebí 9 l vody a 60 kWh elektrické energie.
Jak si vyrobit vodík
Při elektrolýze vody se průchodem elektrického proudu roztokem štěpí vazby mezi vodíkem a kyslíkem a voda se tak rozkládá na tyto dva plyny. Celková účinnost tohoto procesu se pohybuje okolo 55–60 %. Na výrobu 1 kg vodíku elektrolýzou je zapotřebí 9 l vody a 60 kWh elektrické energie.
Co je to Hydrogen
Vodík (chemická značka H, latinsky hydrogenium) je nejlehčí a nejjednodušší plynný chemický prvek. Tvoří převážnou část hmoty ve vesmíru. Elementární vodík (H2) má široké praktické využití: zdroj energie, redukční činidlo v chemické syntéze nebo metalurgii a také jako náplň meteorologických a pouťových balonů a do 30.
Kdy pít elektrolyty
Negativní vliv na příjem elektrolytů má jak dehydratace, tak i nadměrný příjem tekutin. Více by se mělo pít při sportu, v horku a při nemocech, které provází průjem a zvracení.
Jak si doma vyrobit vodík
Při elektrolýze vody se průchodem elektrického proudu roztokem štěpí vazby mezi vodíkem a kyslíkem a voda se tak rozkládá na tyto dva plyny. Celková účinnost tohoto procesu se pohybuje okolo 55–60 %. Na výrobu 1 kg vodíku elektrolýzou je zapotřebí 9 l vody a 60 kWh elektrické energie.
Jakou barvu má vodík
Vodík je bezbarvý, lehký plyn, bez chuti a zápachu.
Jak často pít vodíkovou vodu
Vodíková voda je čistá, bez chuti a zápachu, pouze s malými bublinkami plynu. Doporučujeme pít ji denně. Je vhodná i pro děti, starší lidi, těhotné a kojící ženy. Dosud nebyly zjištěny žádné vedlejší účinky.



0 Comments